Oncologia Molecular
Por meio do sequenciamento de nova geração (NGS), a partir da análise de tecido em bloco de parafina ou sangue, conseguimos identificar mutações genéticas, as quais predispõem o desenvolvimento de tumores. A identificação destas mutações possibilita uma análise completa de risco para o paciente, assim como também possibilita o diagnóstico precoce, prognóstico e tratamento. Dispomos de análise de genes individuais, como, por exemplo, EGFR, BRAF, HER2, IDH, NRAS, KRAS, PDGFRA, KIT, ALK, PIK3CA e ROS1, painéis somáticos pequenos, com genes alvos para determinados tipos específicos de Câncer, como: Câncer de Mama, Melanoma, Colorretal e Pulmão. E painéis somáticos ampliados com múltiplos alvos, que avaliam até 52 genes, como o Painel Oncológico Somático (Ampliseq Focus).
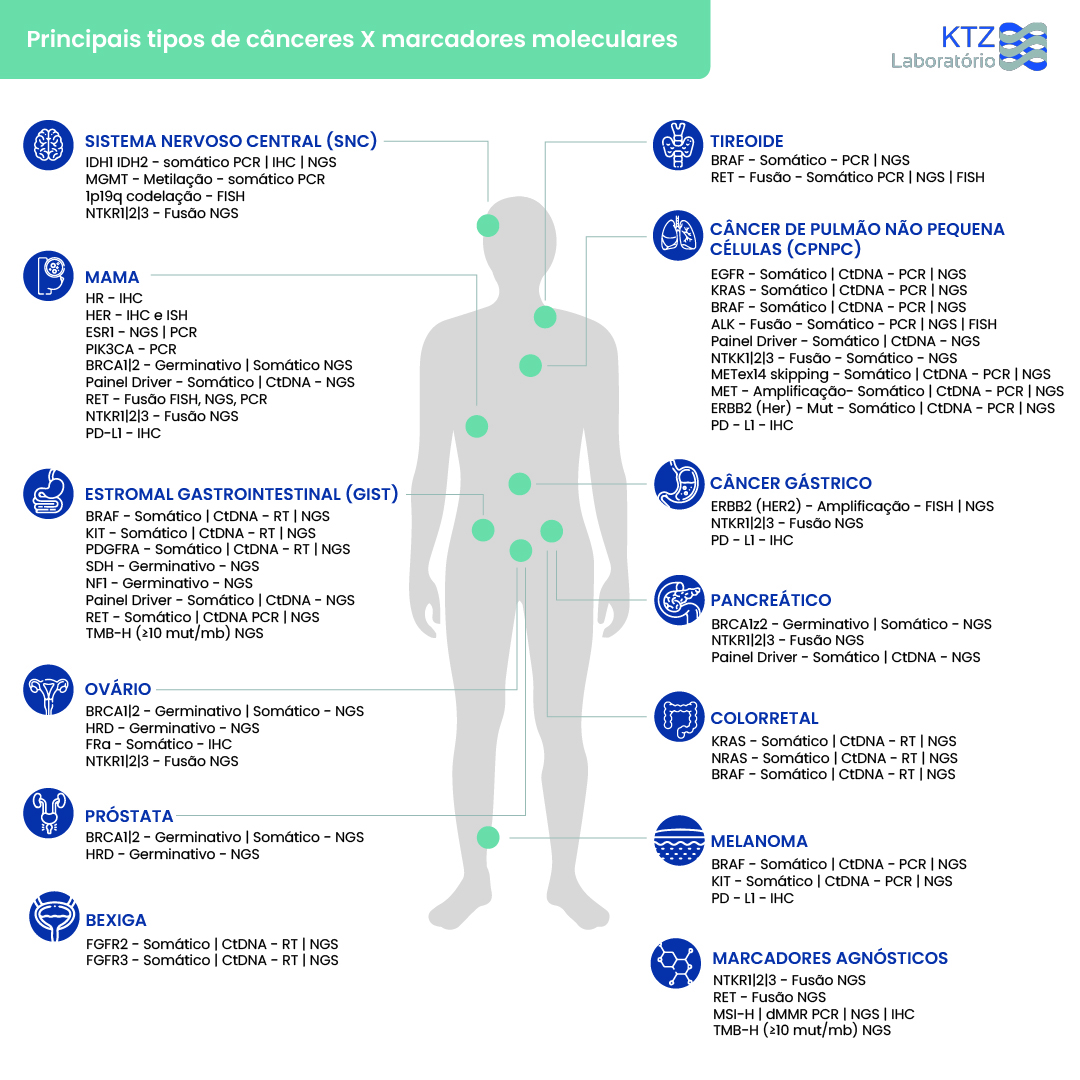
ANÁLISE DO GENE BRAF POR NGS
Código do exame: BRAF
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF. Análise com CNVs, Hotspot genes e Fusion drivers

ANÁLISE DOS GENES BRCA1 E BRCA2
Código do exame: BRCA
Tipo de amostra: Sangue Total
Meios de coleta: Tubo com EDTA (roxo)
Volume: 4mL
Método: SEQUENCIAMENTO NGS COM CNV
Prazo: 20 dias úteis
Observação: Não aplicável.
Descrição do Exame:O câncer de mama e o de ovário estão associados a um componente hereditário em 5 a 10% dos casos. Este tipo de câncer se caracteriza por sua incidência em mulheres jovens, inclusive antes dos 40 anos. A presença de mutações nos genes BRCA1 e BRCA2 é suficiente para que os indivíduos portadores apresentem um maior risco acumulado para desenvolver câncer de mama e/ou ovário ao longo da vida. Foram identificadas mutações nos genes BRCA1 e BRCA2 em até 30% dos casos de câncer de mama hereditário e os pacientes portadores de mutações nos genes apresentam um risco de desenvolver a doença que varia entre 45% e 80%.
Levando em conta o câncer de ovário, o risco oscila entre 20% e 40% para portadoras de mutações em BRCA1 e entre 10% e 20% para portadoras de mutações no gene BRCA2. As mutações nos genes BRCA1 e BRCA2 predispõem, além do câncer de mama (inclusive em homens), aos cânceres de ovário, próstata e pâncreas.

ANÁLISE DO GENE EGFR POR NGS
Código do exame: EGFR
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Gene analisado: EGFR. Análise com CNVs, Hotspot genes e Fusion drivers

ANÁLISE POR GENE HER2 POR NGS
Código do exame: HER2
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado
em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Gene Analisado: HER2 (ERBB2). Análise com CNVs, Hotspot genes e Fusion drivers

ANÁLISE POR GENE PDGFA POR NGS
Código do exame: IDH
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: IDH1 e IDH2. Análise com CNVs, Hotspot genes e Fusion drivers.

ANÁLISE POR GENE KIT POR NGS
Código do exame: KITNG
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E
ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Gene Analisado: KIT. Análise com CNVs, Hotspot genes e Fusion drivers.

ANÁLISE POR GENE PDGFA POR NGS
Código do exame: PDGFA
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: PDGFA. Análise com CNVs, Hotspot genes e Fusion drivers

ANÁLISE POR GENE PIK3C POR NGS
Código do exame: PIK3C
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: PIK3C. Análise com CNVs, Hotspot genes e Fusion drivers.

ANÁLISE POR GENE ROS1 POR NGS
Código do exame: ROS1
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Gene analisado: ROS1. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE PÂNCREAS
Código do exame: PANCR
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: CDK6; CTNNB1; FGFR1; FGFR3; KIT; KRAS; MYC; PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE BEXIGA
Código do exame: PBEXI
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: AKT1; CCND1; EGFR; HER2; FGFR1; FGGR3; HRAS; KRAS; MYC; PIK3CA..
Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE CABEÇA E PESCOÇO
Código do exame: PCABE
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: CCND1; CDK6; EGFR; ERBB2; FGFR1; FGFR3; HRAS; KRAS; MET; NRAS;
PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE ESÔFAGO
Código do exame: PESOF
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: CCND1; CDK6; EGFR; FGFR1; FGFR2; KRAS; MET; MYC; PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE FÍGADO
Código do exame: PFIGA
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; CCND1; CTNNB1; IDH1; IDH2; KRAS; MYC; NRAS. Análise com
CNVs, Hotspot genes e Fusion drivers.

PAINEL CÂNCER DE ESTÔMAGO
Código do exame: PGAST
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: AR; BRAF; CCND1; CDK4; CDK6; EGFR; ERBB2; ERBB3; FGFR2; KRAS;
MET; PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE GLIOBLASTOMA
Código do exame: PGLIO
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; CDK4; CDK6; EGFR; FGFR1; FGFR3; IDH1; KIT; MET; MYCN;
PDGFRA; PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER DE INTESTINO
Código do exame: PINTE
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; CTNNB1; ERBB2 (HER2); ERB3; ESR1; FGFR1; KRAS; MYC; NRAS;
PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers

PAINEL DE CÂNCER DE MAMA
Código do exame: PMAMA
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: AKT1; CCND1; HER2; FGFR1; MYC; NTRK3; PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE MESOTELIOMA
Código do exame: PMESO
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; KIT, PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER PERSONALIZADO
Código do exame: PONCO
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: análise de genes determinada pelo patologista no pedido médico (até 06 genes analisados). Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER DE OVÁRIO
Código do exame: POVAR
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; CCND1; CTNNB1; FGFR1; FGFR3; KIT; KRAS; MYC; PIK3CA. Análise
com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER DE PULMÃO 3 (Não pequenas células)
Código do exame: PPUL3
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: ALK; BRAF; CCND1; CDK4; EGFR; ERBB2; FGFR1; FGFR3; KRAS; MYC;
NTRK1; PIK3CA; RET. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER DE PULMÃO 3 (Pequenas células)
Código do exame: PPUL4
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: EGFR, FGFR1; KRAS; MYC; MYCN, PIK3CA. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE SARCOMA DE TECIDOS MOLES
Código do exame: PPUL4
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: CCDN1; CDK4; ERG; FGFR1; HRAS; KRAS; NRAS; PIK3CA. Painel com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER TESTICULAR
Código do exame: PTEST
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS)
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: BRAF; CTNNB1; FGFR3; HRAS; Painel com CNVs, Hotspot genes e Fusion drivers.

PAINEL DE CÂNCER DE TIREOIDE
Código do exame: THYR
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame: Genes Analisados: AKT1; BRAF; CTNNB1; HRAS; IDH1; KRAS; NRAS; NTRK1; RET.. Análise com CNVs, Hotspot genes e Fusion drivers.

PAINEL ONCOLÓGICO SOMÁTICO - AMPLISEQ FOCUS - NGS
Código do exame: ONCOF
Tipo de amostra: Tecido tumoral
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Volume: N.A
Método: SEQUENCIAMENTO DE NOVA GERAÇÃO (NGS), PCR E ELETROFORESE CAPILAR.
Prazo: 15 dias úteis
Documento adicional: QUESTIONÁRIO – EXAMES GENÉTICOS E TERMO DE
CONSENTIMENTO LIVRE E ESCLARECIDO PARA TESTE GENÉTICO
Observação: É obrigatório o envio da cópia do pedido médico, questionário e termo de consentimento devidamente preenchidos.
Descrição do Exame:
Análise de 52 Genes:
Genes analisados: ABL1 (NM_005157), AKT1 (NM_001014431), AKT3 (NM_005465), ALK (NM_004304), AR (NM_000044), AXL (NM_021913), BRAF (NM_004333), CCND1 (NM_053056), CDK4 (NM_000075), CDK6 (NM_001145306), CTNNB1 (NM_001904), DDR2 (NM_006182), EGFR (NM_005228), ERBB2 (NM_004448), ERBB3 (NM_001982), ERBB4 (NM_005235), ERG (NM_182918), ESR1 (NM_001122740), ETV1 (NM_001163147), ETV4 (NM_001079675), ETV5 (NM_004454), FGFR1 (NM_001174067), FGFR2 (NM_000141), FGFR3 (NM_000142), FGFR4 (NM_213647), GNA11 (NM_002067), GNAQ (NM_002072), HRAS (NM_005343), IDH1 (NM_005896), IDH2 (NM_002168), JAK1 (NM_002227), JAK2 (NM_004972), JAK3 (NM_000215), KIT (NM_000222), KRAS (NM_004985), MAP2K1 (NM_002755), MAP2K2 (NM_030662), MET (NM_000245), MTOR (NM_004958), MYC (NM_002467), MYCN (NM_005378), NRAS (NM_002524), NTRK1 (NM_002529), NTRK2 (NM_006180), NTRK3 (NM_001012338), PDGFRA (NM_006206), PIK3CA (NM_006218), PPARG (NM_015869), RAF1 (NM_002880), RET (NM_020975), ROS1 (NM_002944) e SMO (NM_005631).
Análise com CNVs, Hotspot genes e Fusion drivers.

Painel de Câncer Hereditário por NGS: Precisão e Prevenção na Luta Contra o Câncer
A genética tem um papel fundamental na saúde, e quando o assunto é câncer, essa relação se torna ainda mais evidente. Estima-se que até 10% dos casos de câncer têm origem hereditária, ou seja, são causados por mutações genéticas transmitidas de geração em geração. Identificar essas alterações precocemente pode salvar vidas, permitindo estratégias personalizadas de rastreamento e prevenção.
O Painel de Câncer Hereditário por Sequenciamento de Nova Geração (NGS) é um exame genético avançado que analisa múltiplos genes simultaneamente, investigando variantes associadas a diferentes tipos de câncer hereditário, como de mama, ovário, colorretal, próstata, endométrio, pâncreas, entre outros. Com essa abordagem, é possível detectar predisposições genéticas antes mesmo do desenvolvimento da doença, possibilitando que médicos e pacientes tomem decisões estratégicas para reduzir os riscos.
Para quem o teste é indicado?
O Painel de Câncer Hereditário é altamente recomendado para pessoas que possuem:
– Histórico familiar de câncer precoce (diagnóstico antes dos 50 anos).
– Casos múltiplos de câncer na família, especialmente do mesmo tipo.
– Câncer bilateral ou multifocal, como câncer de mama em ambas as mamas.
– Diagnóstico de câncer raro ou agressivo, como câncer de ovário ou pâncreas.
– Parentes com mutações genéticas já identificadas associadas ao câncer hereditário.
Por que realizar o Painel de Câncer Hereditário?
– Tecnologia avançada e abrangente: O NGS permite analisar diversos genes em um único exame, aumentando a precisão do diagnóstico.
– Plano de rastreamento personalizado: Com o resultado, médicos podem recomendar exames mais frequentes e específicos para cada paciente.
– Prevenção e redução de riscos: Medidas como cirurgias preventivas, terapias-alvo e mudanças no estilo de vida podem ser adotadas para reduzir drasticamente as chances de desenvolver a doença.
– Benefício para toda a família: Se uma mutação é identificada, parentes próximos também podem se beneficiar do rastreamento genético.
Como o exame é feito?
A coleta do material é simples e indolor: pode ser realizada com uma amostra de sangue em EDTA ou swab oral (células da mucosa bucal). O processo é rápido, seguro e não invasivo.
Cuide do seu futuro e da sua família! O conhecimento genético é uma ferramenta poderosa para a saúde preventiva. Se você tem histórico familiar de câncer, converse com seu médico e avalie a necessidade de realizar o Painel de Câncer Hereditário por NGS.
PESQUISA DA MUTAÇÃO FATOR V DE LEIDEN (H1299R e Y1702C)
Código do exame: FATV2
Tipo de amostra: Sangue Total ou Células da mucosa
Meios de coleta: Tubo EDTA K2 (Sangue Total), Swab oral
(Células da mucosa) ou FTA (Gota de Sangue)
Estabilidade da amostra: 5 dias refrigerado de 2°C a 8°C. FTA não é necessário refrigerar.
Volume: 4 ml
Método: PCR em tempo real
Prazo: 3 dias úteis.
Questionário: Termo de Consentimento Livre e Esclarecido para Teste Genético (TCLETG).
Descrição do Exame: O fator de coagulação V é um cofactor enzimático que participa do processo de coagulação em cascata e contribui para o equilíbrio hemostático. Mutações no gene fator V estão entre as causas da trombose
venosa. Outras condições associadas a mutações nos genes do fator V são complicações da gravidez, como abortos. A mutação mais comum no gene fator V é a mutação de Leiden. Outro polimorfismo que ocorre no gene fator V é o polimorfismo A4070G, isto é, a mudança da adenina para guanina para nucleotídeo 4070 que resulta na mudança do aminoácido Histidina para Arginina na posição 1299 da proteína (His1299R / g) e está associada à trombofilia hereditária. Outra mutação relacionada ao fato V é a mutação missense Y1702C, que está associada a deficiência do fator V (FV) com consequente desequilíbrio hemostático, levando à doença hemorrágica.
Diagnóstico de Leucemia e outras doenças
Os exames genéticos baseados em Sequenciamento de Nova Geração (NGS), PCR e Sequenciamento Sanger desempenham um papel essencial no diagnóstico, prognóstico e monitoramento de leucemias e outras doenças hematológicas. Essas técnicas permitem a detecção de mutações específicas e translocações que são fundamentais para personalizar o tratamento e monitorar a resposta terapêutica. Abaixo estão os principais exames utilizando os métodos PCR em tempo real, Sequenciamento Sanger e NGS, classificados de acordo com sua relevância clínica para doenças hematológicas:
1. PCR para BCR-ABL1 (Translocação t(9;22))
Finalidade: Detecta o gene de fusão BCR-ABL1, característico da leucemia mieloide crônica (LMC) e presente em alguns casos de leucemia linfoblástica aguda (LLA). É crucial para o diagnóstico inicial e monitoramento da resposta ao tratamento com inibidores de tirosina quinase.
Utilização: Diagnóstico e monitoramento da doença residual mínima (MRD), com acompanhamento da carga tumoral.
Serviço de Urgência: O laboratório oferece processamento de urgência para este exame por PCR em tempo real, permitindo decisões rápidas e adequação do tratamento.
2. PCR para Mutações FLT3
Finalidade: Detecta mutações no gene FLT3, especialmente a mutação FLT3-ITD, que está associada a um pior prognóstico em leucemia mieloide aguda (LMA). A presença dessa mutação influencia a escolha de tratamentos com inibidores de FLT3.
Utilização: Diagnóstico e orientação terapêutica para o uso de terapias-alvo.
3. PCR para PML-RARA (Translocação t(15;17))
Finalidade: Identifica a fusão gênica PML-RARA, característica da leucemia promielocítica aguda (LPA). A rápida identificação dessa translocação permite o início imediato do tratamento com ácido transretinoico (ATRA) e arsenito de trióxido, essencial para o manejo dessa emergência médica.
Serviço de Urgência: Disponibilizamos processamento de urgência para o exame PML-RARA via PCR em tempo real, dada a criticidade do início imediato do tratamento.
4. Painel de NGS que avalia Mutações no Gene TP53
Finalidade: Analisa mutações no gene TP53, frequentemente associadas a formas agressivas de leucemia, como LMA e leucemia linfocítica crônica (LLC). Mutações neste gene indicam um prognóstico reservado e podem demandar abordagens terapêuticas mais intensivas.
Utilização: Avaliação prognóstica e planejamento de tratamentos mais agressivos ou experimentais.
5. Painel NGS que avalia Mutações nos Genes RAS (NRAS e KRAS)
Finalidade: Identifica mutações nos genes NRAS e KRAS, comumente envolvidas na regulação da proliferação celular. Essas mutações estão associadas a casos de LMA e podem guiar a escolha de terapias experimentais ou direcionadas.
Utilização: Prognóstico e potencial participação em ensaios clínicos com terapias-alvo.
6. Sequenciamento Sanger para Mutações JAK2 V617F
Finalidade: Detecta a mutação JAK2 V617F, frequentemente associada a neoplasias mieloproliferativas, como policitemia vera, trombocitemia essencial e mielofibrose primária. A mutação ativa a via de sinalização JAK-STAT, promovendo a proliferação celular desregulada.
Utilização: Diagnóstico e monitoramento dessas neoplasias mieloproliferativas, auxiliando na estratificação do risco e na escolha de tratamentos específicos.
Os exames genéticos utilizando NGS, Sequenciamento Sanger e PCR em tempo real são ferramentas indispensáveis para o manejo clínico das leucemias e outras doenças hematológicas, permitindo uma abordagem terapêutica precisa e personalizada. Nosso laboratório está equipado para oferecer serviço de urgência para os exames BCR-ABL1 e PML-RARA, garantindo que o diagnóstico e tratamento possam ser agilizados em situações críticas.
Os exames BCR/ABL e PML-RARA são essenciais para o diagnóstico e monitoramento de leucemias, como leucemia mieloide crônica (LMC) e leucemia promielocítica aguda (LPA). Utilizando PCR, é possível detectar translocações genéticas específicas com alta sensibilidade, permitindo um diagnóstico precoce e preciso. Os principais benefícios incluem a possibilidade de monitorar a resposta ao tratamento e ajustar a terapia conforme necessário. A detecção dessas fusões genéticas é crucial para a escolha de terapias direcionadas, aumentando as chances de remissão e melhorando o prognóstico dos pacientes.
Para o serviço de processamento de urgência é cobrado uma taxa de urgência pelo processamento em até 24 horas.
BCR/ABL - QUALITATIVO P190 P210 DIAGNÓSTICO DE LEUCEMIA CROMOSSOMA PHILADELPHIA
Código do exame: BCRQL
Tipo de amostra: SANGUE TOTAL OU ASPIRADO DE MEDULA ÓSSEA
Meios de coleta: Tubo com EDTA (roxo)
Estabilidade da amostra: A amostra é estável por até 48 horas refrigerada de 2°C a 8°C.
Volume: 16 mL (Sangue Total) 4 mL (Medula Óssea)
Método: PCR em tempo real
Prazo: 7 dias úteis
Documento adicional: FORMULÁRIO PARA ANÁLISES ONCOHEMATOLÓGICAS
Descrição do Exame: Este exame detecta o transcrito do produto de fusão de parte do oncogene ABL com o gene BCR, proveniente da translocação entre os cromossomos 9 e 22 (cromossomo Filadélfia – Ph). Esta fusão,
denominada translocação BCR/ABL, dá origem a duas isoformas que codificam as proteínas p210 e p190.

DETECÇÃO DA FUSÃO PML-RARA (15:17)
Código do exame: PML-RARA
Tipo de amostra: SANGUE TOTAL OU ASPIRADO DE MEDULA ÓSSEA
Meios de coleta: Tubo com EDTA (roxo)
Estabilidade da amostra: A amostra é estável por até 48 horas refrigerada de 2°C a 8°C.
Volume: 24 mL (Sangue Total)/4 mL (Medula Óssea)
Método: PCR em tempo real
Prazo: 7 dias úteis
Documento adicional: FORMULÁRIO OBRIGATÓRIO
Descrição do Exame: O gene PML é um gene supressor de tumor envolvido no controle da estabilidade genômica. A oncoproteína PML-RAR é o produto da translocação t(15;17), ela interrompe o processo de diferenciação das células mieloides, bloqueando a maturação mieloide no estágio de promielócitos, o que pode ser um dos primeiros passos no processo de leucemogênese. Este estado caracteriza a Leucemia Promielocítica, também denominada M3.

JAK-2 PESQUISA DA MUTAÇÃO V617F DO EXON 14
Código do exame: JAK2
Tipo de amostra: Sangue Total ou Células da mucosa
Meios de coleta: Tubo EDTA K2 (Sangue Total), Swab
oral (Células da mucosa) ou FTA (Gota de Sangue)
Estabilidade da amostra: 5 dias refrigerado de 2°C a
8°C. FTA não é necessário refrigerar
Volume: Sangue total: 4 ml / medula: 1 ml
Método: SEQUENCIAMENTO SANGER
Prazo: 9 dias úteis
Questionário: Termo de Consentimento Livre e
Esclarecido para Teste Genético (TCLETG).
Descrição do Exame: A variante V617F é uma mutação pontual, com substituição do nucleotídeo Guanina (G) por Timina (T) no éxon 14 do gene JAK2, ocasionando a substituição do aminoácido Valina (V) pela Fenilalanina (F) na posição 617 (V617F). Essa mutação é de caráter somático (mutação adquirida), sendo detectada em células de linhagem eritróide e mieloide, porém não detectada em células T ou células da mucosa oral. A JAK2 V617F está associada à sinalização intracelular exacerbada e à proliferação eritróide, podendo estar envolvida na gênese de síndromes mieloproliferativas, como Policitemia Vera, Trombocitemia Essencial e Mielofibrose Idiopática. A pesquisa da mutação JAK2 V617F em pacientes com síndromes mieloproliferativas é de suma importância para definir a melhor conduta clínica.
Para o serviço de processamento de urgência é cobrado uma taxa de urgência pelo processamento em até 24 horas.
Instabilidade por microssatélites (MSI)
O exame de instabilidade por microssatélites (MSI) é utilizado principalmente para identificar instabilidades genômicas em tumores, especialmente no câncer colorretal. Essas instabilidades são características de defeitos no sistema de reparo do DNA, comumente associados à síndrome de Lynch, uma forma hereditária de predisposição ao câncer. O teste de MSI ajuda a determinar o perfil genético do tumor, orientar decisões terapêuticas, e identificar pacientes e familiares com risco aumentado para desenvolver certos tipos de câncer, auxiliando no planejamento de estratégias de monitoramento e prevenção.
Realizamos o exame instabilidade por microssatélites (MSI), utilizando PCR e eletroforese capilar, técnicas que permitem detectar variações em repetições curtas de DNA com alta sensibilidade. As principais vantagens incluem a precisão na identificação de alterações genéticas associadas a síndromes como o câncer colorretal hereditário. Marcadores comuns incluem BAT-25, BAT-26 e NR-21. A acurácia do PCR e eletroforese capilar é elevada, muitas vezes superando a imuno-histoquímica, especialmente na detecção de instabilidades em regiões genômicas específicas que podem passar despercebidas em análises baseadas em proteínas.
INSTABILIDADE DE MICROSSATÉLITES
Código do exame: IMS
Tipo de amostra: TECIDO TUMORAL
Meios de coleta: Bloco de parafina
Estabilidade da amostra: A amostra é estável por tempo indeterminado em temperatura ambiente.
Método: PCR E ELETROFORESE CAPILAR
Prazo: 5 dias úteis.
Documento adicional: Termo de Consentimento Livre e Esclarecido (TCLE)
Observação: É obrigatório envio da cópia do pedido médico, cópia do laudo anatomopatológico e termo de consentimento corretamente preenchidos.

